سیستم های ترشحی در باکتری ها | کافه پزشکی
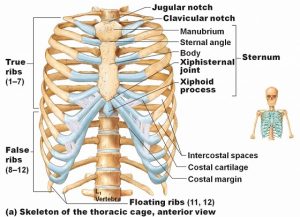
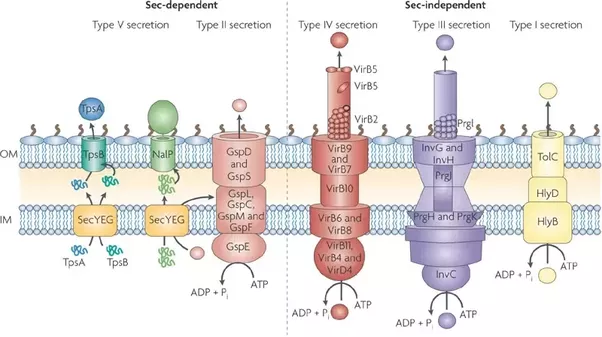
ترشح پروتئین نقش محوری در تعدیل اثر متقابل باکتری با محیط خود دارد. این امر به ویژه در مورد زمانی که باکتری همزیست (چه بیماری زا، کامنسال یا موچوالیست ) در تعامل با میزبان بزرگتر می باشد در مورد باکتری های گرم منفی ترشح نیاز به انتقال از غشای داخلی و همچنین غشای خارجی و تنوع سیستمهای مولکولی برای این منظور است. باکتری ها برای این منظور مجهز به چندین نوع سیستم ترشحی شده اند. همراه کافه پزشکی باشید
سیستم ترشحی نوع I :
عبور پروتئین های ترشحی در یک مرحله از غشاء داخلی و خارجی انجام می گیرد. (بدون واسطه ی پری پلاسمی)
این نوع ترشح نیاز به ۳ پروتئین دارد:
- ABC) ATP_binding Cassette ) که در غشاء داخلی است.
- پروتئین در غشاء خارجی (OMP )
- پروتئین فیوژن (MFP ) که فضای پری پلاسمیک را در بر می گیرد. اطلاعات درون ۶۰ اسید آمینه انتهایی در –COOH قرار می گیرد.
این مسیر وابسته به سیستم Sec و پروسه آمینو ترمینال نیست.
آنچه در این پست کافه پزشکی خواهید دید
سیگنال ترشحی
در انتهای C – terminal
شناسایی اختصاصی پروتئین ABC
سبب راه اندازی و assemble شدن کمپلکس انتقال غشایی
تکرارهای غنی از گلیسین
اتصال اختصاصی به یونهای کلسیم و ایجاد ساختارهای ساندویچی و بتا رول
در طول ترشح جدا نمی شود.
برخی ویژگیهای پروتئینهای ترشحی تیپ یک :
اندازه متنوع : از ۷۸ تا ۸۶۸۲ اسید آمینه تشکیل شده اند.
عملکرد متنوع : شامل انواع هیدرولازها تا توکسینهای سمی
اکثرا اسیدی
فاقد سیستئین یا خیلی کم
- ATP_binding Cassette
- Tol C/ OMP
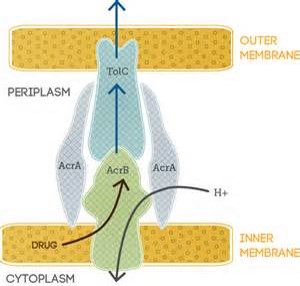
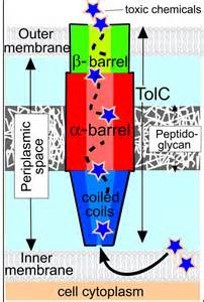
MFP
دارای یک قطعه N-terminal کوتاه در سیتوپلاسم
یک قطعه منحصر به فرد بین غشایی(transmembrane)
یک قطعه پری پلاسمیک بزرگ
ایجاد نیروی مکانیکی وارد بر دومین استوایی Tol C
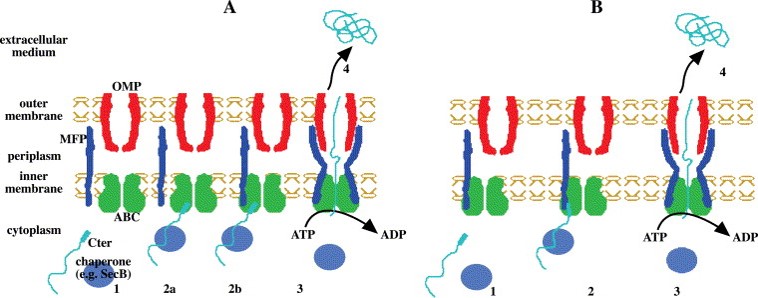
سیستم ترشحی تیپ II :
- به طور وسیع در باکتریهای گرم منفی
- با دخالت مسیر Sec
- نیاز به پپتید N- terminal
- انتقال پروتئین از سیتوپلاسم به فضای پری پلاسمیک و شکسته شدن پپتید سیگنال
- تبدیل پروتئین به شکل ثانویه و احتمالا سومین ساختار قبل از عبور از میان غشای خارجی توسط سیستم ترشحی تیپ دو انجام می شود.
- مشارکت حداقل ۱۲ ژن
- استفاده بسیاری از پاتوژنهای گیاهی و جانوری حهت خروج اگزوتوکسینها و آنزیمهای مهم هیدرولیتیک
بهترین سیستم ترشحی تیپ دو که تاکنون شناخته شده است سیستم Pul کلبسیلا اکسی توکا در ترشح پولوناز می باشد. سایر سیستمهای ترشحی شامل سیستم Xcp سودوموناس آئروزینوزا که الاستاز- اگزوتوکسین A و فسفو لیپاز C را ترشح می کند. مسیر Esp در ترشح توکسین وبا و در ویبریو کلرا دخالت دارد.
سیستم Out که انزیمهای پکتیناز و سلولازها را در اروینیا کریستانتمی ترشح می کند و مسیر Exe در ترشح آمیلاز و پروتئاز آئروموناس هیدروفیلا دخالت دارند.
پروتئینهایی که توسط این سیستم ترشح می شوند به صورت پیش پروتئین در ریبوزومهای سیتوپلاسمی ساخته شده و دارای یک توالی سیگنال هستند.
سیستم Sec در E.coli شامل SecA-SecB-SecD-SecY-SecF می باشد که SecA به عنوان ATPase عمل کرده و انرزی لازم برای خارج کردن پروتئین ترشحی توسط چاپرون SecB را فراهم می کند.
عبور پروتئین ها در دو مرحله انجام میشود. این پروتئین ها به صورت پیش پروتئین ساخته شده و دارای سکانس سیگنال یا راهنما در انتهای آمینی خود حاوی ۴۰-۱۵ اسیدآمینه هستند. این پروتئین در حین عبور از غشاء داخلی نیاز به سیستم SEC دارند. عده ای از این پروتئین های غشاء داخلی مانند
sec D,F,Y و ATP آز که Sec A است. Sec B نقش چاپرون را دارد که به سیگنال پپتیداز و پروپروتئین اتصال یافته و بعد از انتقال قطعه اضافی، توسط پپتیداز جدا شده (LSPA) و پروتئین کامل به درون فضای پری پلاسمیک آزاد میشود. در غشاء خارجی پروتئین هایی هستند که باعث انتقال به خارج سلول میشود.
مسیر tat در باکتری های گرم منفی و مثبت جهت انتقال پروتئین ها از خلال غشا نقش دارد. در باکتری های گرم منفی این سیستم پروتئین های را به سیستم ترشحی ۲ تحویل می دهد تفاوت این سیستم از سیستم sec در این است که tat تنها پروتئین های چین خورده را انتقال می دهد.
سیستم ترشحی تیپ III :
سیستم وابسته به پاتوژنیسیسته به طور گسترده در باکتریهای گرم منفی یافت میشود : ترشح پروتئینهای سنتز شده سیتوپلاسمی از عرض دو لایه پوشش سلولی.در پاتوژنهای گرم منفی این سیستمها معمولا درگیر در ترشح فاکتورهای ویرولانس هستند.بسیاری از این پروتئینها در خارج کردن پروتئینهای تاژهای باکتریایی درگیر هستند.برخی سیستمهای تیپ ۳ که کمپلکسهای پروتئینی هستند و مانند سوزنهای هیپودرمیک عمل میکنند میتوانند پروتئینها را مستقیما به سیتوپلاسم میزبان تزریق کنند بدون این که این پروتئینها در معرض محیط خارج سلول قرار بگیرند.این حقیقت دلالت دارد بر حضور یک کمپلکس منفذ پروتئینی باکتریایی که میتواند غشاهای برخی سلولهای میزبانی را در بر بگیرد و به ابزارهای ترشح باکتریایی متصل است.این سیستمهای ترشحی پروتئینهایی با کمبود توالی سیگنال را انتقال میدهند که برای ترشح به چاپرونهای اختصاصی نیاز دارد.
این سیتم غیر وابسته به Sec می باشد. سیستم ترشحی تیپ ۳ با تماس باکتری با سطح میزبان فعال می شود.
چاپرونها با اتصال به پروتئینهای ترشحی مانع از واکنش پروتئینهای پیش ساز با سایر پروتئینها شده و از ساختمان آنها محافظت می کنند.
پاتوژنهای حیوانی استفاده کننده از این سیستم انواع یرسینیا-شیگلا فلکسنری-سالمونلا تیفی موریوم- اشیریشیا کلی انتروپاتوژنیک- انواع کلامیدیا و از پاتوژنهای گیاهی مانند سودوموناس سیرینژیه-انواع اروینیا-گزانتوموناس کمپستریس و انواع ریزوبیوم
TTSS ها در وابستگی ترشح به سیگنالهای خارجی عموما ارتباط با سلول میزبان منحصر به فرد هستند.مکانیسم صادر کننده TTSS معمولا متشکل از ۲۰ پروتئین مختلف و شامل پروتئینهای محلول سیتوپلاسمی،پروتئینهای غشای خارجی و پروتئینهای غشای داخلی است.TTSS ها باکتریها را قادر میسازند که یک تنوعی از افکتورها را مستقیما به سیتوزول میزبان بفرستند و باعث دستکاری پروسههای سلولی میزبان شوند و برای مزایای خود آنها را از درون تخریب کنند.
ژنهای کد کننده سیستم ترشحی تیپ IIIروی عناصر ژنتیکی غیر پایدار،پلاسمید و جزایر پاتوژنیسیته واقع شدهاند شامل hrp-PAI در Pseudomonas syringae.
در Peudomonas syringae مانند سایر پاتوژنهای گیاهی ژنهای کد کننده TTSS درون یک جزیره پاتوژنیسیته دسته بندی میشوند.
سیستم ترشحی Hrp در P.syringae
ژنهای hrp در پاتووار P.syringae در یک منطقه کروموزومی دستهبندی شدهاند شامل بیش از ۲۷ ژن hrp سازماندهی شده در ۷ اپرون کد کننده پروتئینهای افکتور،ترشحی یا تنظیمی.۹ تا از ژنهای hrp در میان پاتوژنهای باکتریایی مختلف گیاهان و جانوران حفاظت شدهاند و به hrc تغییر نام یافتهاند.این ژنهای hrc شامل hrcC,hrcN,hrcJ,hrcQ,hrcR,hrcS,hrcT,hrcU,hrcV هستند.۸ تا از ژنهای hrc در سطح غشای داخلی قرار گرفتهاند و یک منفذ محافظت شده مشابه بازال بادی را شکل میدهند.حدس زده میشود که منفذ میتواند در شناسایی یک سیگنال ترشحی عمومی درگیر باشد.hrcC یک استثنا است وابسته به خانواده secretin و به عنوان یک پروتئین تشکیل دهنده منفذ در غشای خارجی عمل میکند.
تنظیم بیان ژنهای hrp و ترشح
HrpL یک سیگما فاکتور است که تمام ژنهای hrp وavr را با شناسایی یک توالی حفاظت شده bp 26که hrp-box نامیده میشود شناسایی میکندGGAACC-N16-CCAC ،که در بالادست بسیاری از ژنهای avr وhrp حضور دارند.آنالیز شبکه تنظیمی مرتبط با TTSS hrp نشان داد که HrpR وHrps پروتئینهای اتصالی افزایش دهندهای هستند که با DNA میانکنش میدهند تا یک کمپلکس فعالسازی را برای پروموتور hrpL شکل دهند.این دو پروتئین یک هترودایمر را شکل میدهند که به پروموتور hrpL متصل میشود و رونویسی آن را فعال میسازد.
ساختار پیلوس Hrp و عملکرد آن
HrpA یک پروتئین اسیدی ۱۱۳ آمینو اسیدی است و به تنهتیی برای تشکیل ساختارهای فیلامنتی کافی است؛تایید کننده این مطلب که HrpA تنها پروتئین ساختاری یا پروتئین اصلی ساختاری پیلوس Hrp است.پیلوس Hrp به عنوان یک لوله هدایت کننده پروتئینها از عرض دیواره سلولی گیاهی به سیتوپلاسم میزبان عمل میکند.توسعه قطبی زایده از طریق افزودن دور زیرواحدهای HrpA به انتهای فیلامنت،به پیلوس اجازه نفوذ به دیواره سلولی گیاهی را میدهد.
پروتئین HrpA کارا برای ترشح هارپین HrpW و Avrpto در محیط کشت مورد نیلز است.از نظر مورفولوژیکی پیلی Hrp به نظر انعطاف پذیر میرسد در حالی که سوزن T3SS در پاتوژنهای گیاهی به نظر سخت است.
پروتئینهای ترشح شده از طریق سیستم ترشحی Hrp
سیستم ترشحی Hrp در P.syringae دو خانواده مهم پروتئینها را ترشح میکند:
خانواده اول شامل هارپینهایی مانند HrpZ وHrpW (که در درون PAI کد میشوند)و به درون آپوپلاست (فضاهای درون سلولی )ترشح میشوند.هارپینها میتوانند HR را در درون سلولهای غیر میزبان ایجاد کنند.
خانواده دوم شامل پروتئینهای Avr/Effector میباشند که درون سلولهای گیاهی عمل میکنند و در پاتوژنیسیته در گیاهان میزبان عمل میکنند.
پروتئینهای هارپین
HrpZ درP.syringae به غشای پلاسمایی گیاه متصل میشود و نفوذ و هدایت یون را در دو لایه لیپیدی مصنوعی شکل میدهند.این یافتهها پیشنهاد میکنند که هارپینها میتوانند در آزاد سازی مواد غذایی از سلول میزبان درگیر باشند یا این که آنها میتوانند یک پروتئین کمکی فرضی سیستم ترشحی باشند و در تغییر شکل دیواره سلولی گیاهی در طی انتقال پروتئینهای Avr عمل کنند.
پروتئینهای Avr/Effector
سویههای P.syringae شامل چندین ژن avr هستند که نه تنها در دستههای ژنی hrp/hrc قرار گرفتهاند بلکه در فضاهایی نزدیک به آن نیز قرار دارند.یک Hrp system کارا برای فعالیت کامل پروتئینهای Avr مورد نیاز است
سیستم ترشحی تیپ ۴ (T4SS)
کمپلکسهای پروتئینی بزرگی که از پوشش سلولی بسیاری از باکتریها گذر می کنند.آنها شامل یک کانال هستند کهاز طریق آن پروتئینها یا کمپلکسهای نوکلئوپروتئینی را می توانند انتقال دهند.
انتقال توسط تعدادی از ATPase های سیتوپلاسمیک
بسیار متنوع
سبب انتقال افقی زنها و ایجاد انطباق با تغییرات محیطی و گسترش مقاومت انتی بیوتیکی
انتقال منومرهای پروتئینی – سموم چند زیر واحدی و کمپلکسهای نوکلئوپروتئینی
عملکردها:
کانجوگیشن
ترانسفورمیشن
انتقال پروتئین
ساختمان
IV A پلاسمید Ti باکتری A.tumefaciens و پلاسمید Pk101 باکتری
E. coli
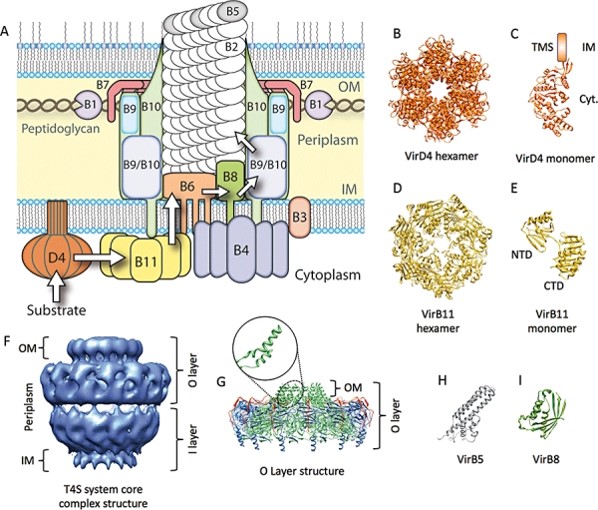
سیستم Ti شامل ۱۲ پروتئین VirB1_VirB11 و VirD4 که VirB/D4 نام دارد.
بخش عمدهای از پروتئین ها (VirB6_VirB10 و VirB3 ) ایجاد داربست کانال انتقال را می دهند.
VirB7-B9-B10 تشکیل کمپلکس هسته (۱۴کپی از هر پروتئین) انتقال که هر دو غشا را می پوشانند.
ترشح پروتئین در باکتریهای گرم مثبت
SecYEG به عنوان کانال جابجایی
ATPaseSecA سیتوپلاسمی برای هل دادن پیش سازهای پروتئینی به داخل کانال
کمپلکس SecDF/YajC برای آزاد سازی از ترانسلوکون
سیگنال پپتیدازها جهت آزاد کردن پلی پپتیدهای بالغ
وجود لیپوپروتئین پپتیدیل –پرولیل ایزومراز برای ترشح برخی پلی پپتیدها به محیط خارج سلولی
منبع : اختصاصی کافه پزشکی